Chủ đề natron chemische formel: Natron, với công thức hóa học Na₂CO₃, là một hợp chất quan trọng trong nhiều lĩnh vực từ công nghiệp sản xuất đến đời sống hàng ngày. Bài viết này sẽ cung cấp cho bạn cái nhìn tổng quan về Natron, bao gồm công thức hóa học, ứng dụng, tính chất và các nghiên cứu khoa học liên quan. Hãy cùng khám phá những lợi ích và ứng dụng đa dạng của Natron trong các ngành công nghiệp và đời sống!
Mục lục
- 1. Tổng quan về Natron (Na₂CO₃)
- 2. Ứng dụng của Natron trong đời sống và công nghiệp
- 3. Natron trong hóa học: Tính chất và phản ứng hóa học
- 4. Lịch sử phát hiện và nghiên cứu về Natron
- 5. Natron trong cuộc sống hàng ngày và trong gia đình
- 6. Các lưu ý khi sử dụng Natron
- 7. Các bài viết, tài liệu tham khảo và nguồn thông tin thêm
1. Tổng quan về Natron (Na₂CO₃)
Natron, hay còn gọi là natri cacbonat, là một hợp chất hóa học có công thức hóa học là Na₂CO₃. Đây là một muối vô cơ được tạo thành từ natri (Na) và anion cacbonat (CO₃²⁻). Natron là một hợp chất phổ biến và có vai trò quan trọng trong nhiều ngành công nghiệp, từ sản xuất xà phòng, thủy tinh, đến xử lý nước và thực phẩm. Bài viết dưới đây sẽ cung cấp cái nhìn chi tiết về công thức hóa học, cấu trúc phân tử và các đặc tính quan trọng của Natron.
1.1. Định nghĩa Natron
Natron là một hợp chất muối có chứa ion natri và ion cacbonat. Công thức hóa học của Natron là Na₂CO₃, với mỗi phân tử Natron bao gồm hai ion natri (Na⁺) và một ion cacbonat (CO₃²⁻). Trong tự nhiên, Natron được tìm thấy ở các hồ nước có độ mặn cao và được sử dụng trong nhiều ứng dụng công nghiệp và gia đình.
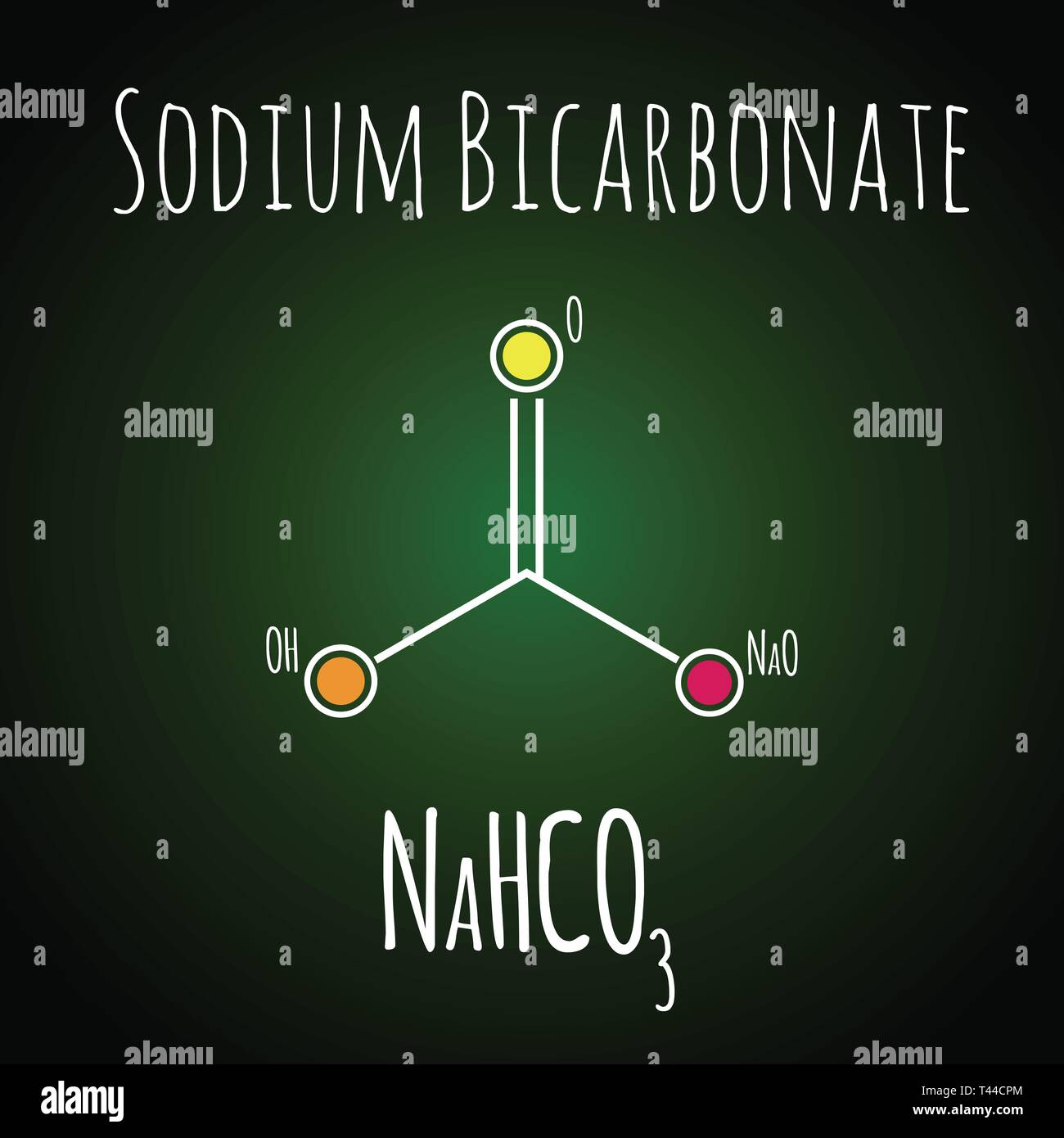
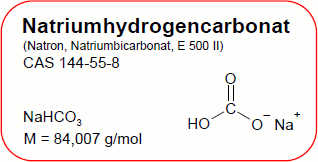
1.2. Công thức hóa học và cấu trúc phân tử
Công thức hóa học của Natron là Na₂CO₃, có nghĩa là mỗi phân tử Natron bao gồm:
- Hai ion natri (Na⁺)
- Một ion cacbonat (CO₃²⁻)
Cấu trúc phân tử của Natron đơn giản nhưng rất quan trọng đối với các ứng dụng hóa học. Ion cacbonat (CO₃²⁻) trong Natron có cấu trúc hình học phẳng, với một nguyên tử cacbon ở trung tâm, liên kết với ba nguyên tử oxy. Các ion natri (Na⁺) được liên kết với ion cacbonat thông qua lực tĩnh điện.
Phản ứng của Natron trong nước có thể tạo thành dung dịch kiềm yếu, với pH khoảng 11. Đây là đặc điểm quan trọng trong các ứng dụng công nghiệp, đặc biệt là trong sản xuất chất tẩy rửa và xử lý nước.
1.3. Các dạng của Natron
Natron có thể tồn tại dưới nhiều dạng khác nhau, với phổ biến nhất là dạng khan (Na₂CO₃) và dạng ngậm nước (Na₂CO₃·10H₂O). Dạng ngậm nước của Natron là dạng tinh thể trong suốt, dễ dàng hòa tan trong nước, và có đặc tính hút ẩm rất mạnh.
1.4. Tính chất vật lý của Natron
- Vị trí hóa học: Muối vô cơ.
- Màu sắc: Natron khan thường có màu trắng hoặc xám nhạt.
- Điểm nóng chảy: Natron khan có điểm nóng chảy khoảng 851°C, trong khi dạng ngậm nước có thể nóng chảy ở nhiệt độ thấp hơn.
- Độ hòa tan trong nước: Natron dễ dàng hòa tan trong nước, tạo ra dung dịch kiềm với pH cao.
Những tính chất này làm cho Natron trở thành một hợp chất quan trọng trong nhiều quy trình sản xuất và trong các ứng dụng xử lý môi trường.
.png)
2. Ứng dụng của Natron trong đời sống và công nghiệp
Natron, với công thức hóa học Na₂CO₃, không chỉ là một hợp chất quan trọng trong ngành công nghiệp mà còn có nhiều ứng dụng hữu ích trong đời sống hàng ngày. Dưới đây là những lĩnh vực mà Natron được sử dụng rộng rãi:
2.1. Ứng dụng trong công nghiệp sản xuất xà phòng và chất tẩy rửa
Natron là một thành phần quan trọng trong quá trình sản xuất xà phòng và chất tẩy rửa. Trong ngành công nghiệp này, Natron được sử dụng để tạo ra dung dịch kiềm mạnh, giúp làm sạch và tẩy rửa các vết bẩn, dầu mỡ. Nó có thể hòa tan trong nước và làm giảm độ axit của dung dịch, từ đó nâng cao khả năng làm sạch. Natron cũng được sử dụng để sản xuất các loại xà phòng giặt và xà phòng vệ sinh.
2.2. Vai trò trong ngành thủy tinh và sản xuất kính
Trong ngành thủy tinh, Natron đóng vai trò quan trọng trong việc giảm nhiệt độ nóng chảy của các thành phần thủy tinh khác như cát silic (SiO₂). Natron giúp giảm chi phí năng lượng trong quá trình sản xuất thủy tinh, đồng thời giúp thủy tinh có độ trong suốt cao hơn. Nó được sử dụng trong sản xuất kính, gạch chịu nhiệt, và các vật liệu chịu nhiệt khác.
2.3. Natron trong công nghệ thực phẩm và y tế
Natron là một thành phần được sử dụng trong ngành công nghệ thực phẩm, đặc biệt là trong sản xuất các loại bánh mì và đồ nướng. Nhờ tính chất kiềm của nó, Natron giúp làm nở bột trong quá trình nướng, tạo ra cấu trúc bánh xốp nhẹ và mềm. Ngoài ra, Natron cũng được sử dụng trong y tế dưới dạng thuốc kháng acid để trung hòa acid dạ dày và giúp giảm các triệu chứng trào ngược axit.
2.4. Ứng dụng trong xử lý nước và làm sạch môi trường
Natron có vai trò quan trọng trong việc xử lý nước thải và làm sạch môi trường. Nó được sử dụng để điều chỉnh độ pH của nước, làm giảm độ axit của nước và giúp cải thiện chất lượng nước. Trong quá trình xử lý nước thải, Natron giúp loại bỏ các ion kim loại nặng và các chất ô nhiễm khác. Natron cũng được sử dụng để làm sạch bề mặt trong các ngành công nghiệp, giúp loại bỏ vết bẩn cứng đầu và cải thiện hiệu quả làm sạch.
2.5. Ứng dụng trong nông nghiệp
Trong nông nghiệp, Natron được sử dụng như một loại phân bón tự nhiên giúp cải thiện tính chất của đất. Nó giúp điều chỉnh độ pH của đất, làm giảm độ chua, tạo môi trường lý tưởng cho cây trồng phát triển. Natron cũng được sử dụng trong việc xử lý các bệnh nấm và vi khuẩn gây hại cho cây trồng, giúp bảo vệ mùa màng mà không gây hại cho môi trường.
2.6. Ứng dụng trong gia đình
Natron còn được sử dụng rộng rãi trong gia đình như một sản phẩm làm sạch và khử mùi. Bạn có thể sử dụng Natron để làm sạch bề mặt nhà bếp, tẩy rửa đồ dùng, thậm chí là khử mùi trong tủ lạnh hoặc tẩy trắng quần áo. Nhờ vào tính năng không độc hại, Natron trở thành lựa chọn an toàn cho việc làm sạch và bảo vệ sức khỏe trong gia đình.
3. Natron trong hóa học: Tính chất và phản ứng hóa học
Natron (Na₂CO₃), một muối vô cơ, sở hữu nhiều tính chất hóa học đặc biệt và tham gia vào một số phản ứng quan trọng. Dưới đây là các tính chất và phản ứng hóa học tiêu biểu của Natron:
3.1. Tính chất vật lý và hóa học của Natron
- Tính chất vật lý:
- Natron là một hợp chất rắn, có màu trắng và dễ hòa tan trong nước.
- Điểm nóng chảy của Natron khan là khoảng 851°C, và nó có thể tồn tại ở dạng ngậm nước (Na₂CO₃·10H₂O) khi có độ ẩm cao.
- Natron có tính kiềm mạnh, khi hòa tan trong nước, tạo ra dung dịch kiềm với pH lên đến 11.
- Tính chất hóa học:
- Natron có khả năng phản ứng với axit để tạo ra muối và nước. Ví dụ, khi phản ứng với axit hydrochloric (HCl), nó tạo ra khí CO₂, nước và muối NaCl:
Na₂CO₃ + 2HCl → 2NaCl + H₂O + CO₂ ↑
- Natron cũng phản ứng với các muối kim loại để tạo thành các muối mới. Phản ứng với muối canxi có thể tạo ra canxi cacbonat (CaCO₃), một hợp chất ít tan trong nước:
Na₂CO₃ + CaCl₂ → CaCO₃ ↓ + 2NaCl
3.2. Các phản ứng hóa học đặc trưng của Natron
Natron tham gia vào một số phản ứng hóa học đặc trưng, trong đó bao gồm các phản ứng với axit và muối, giúp làm rõ tính kiềm của nó và khả năng tác động đến môi trường xung quanh:
- Phản ứng với axit: Natron phản ứng mạnh với các axit, tạo ra muối, nước và khí CO₂. Đây là một phản ứng đặc trưng khi Natron được sử dụng trong các ứng dụng như nấu ăn (tạo bọt khi làm bánh) hay trung hòa axit trong cơ thể.
- Phản ứng trong quá trình sản xuất thủy tinh: Natron được dùng làm chất trợ tan trong quá trình nấu thủy tinh. Trong đó, Natron giúp giảm nhiệt độ nóng chảy của cát silic và làm giảm độ nhớt của thủy tinh.
- Phản ứng với kim loại kiềm: Natron phản ứng với kim loại kiềm (như natri, kali) để tạo ra cacbonat kim loại tương ứng, điều này hữu ích trong việc sản xuất các hợp chất khác của kim loại và trong xử lý các chất thải hóa học.
3.3. Phản ứng phân hủy nhiệt của Natron
Natron cũng có thể bị phân hủy khi nung nóng ở nhiệt độ cao, đặc biệt là trong môi trường không có nước. Quá trình phân hủy này dẫn đến việc tạo ra cacbon dioxide (CO₂) và natri oxit (Na₂O). Phản ứng này là một phản ứng quan trọng trong các ngành công nghiệp chế biến hóa chất:
Na₂CO₃ → Na₂O + CO₂ ↑
3.4. Vai trò của Natron trong các phản ứng acid-base
Với tính kiềm của mình, Natron thường được sử dụng để trung hòa các axit trong các phản ứng acid-base. Khi hòa tan trong nước, Natron cung cấp ion cacbonat (CO₃²⁻), giúp giảm nồng độ của ion H⁺ trong dung dịch, từ đó làm tăng pH và tạo ra môi trường kiềm cần thiết cho các phản ứng khác.
3.5. Sử dụng Natron trong các phản ứng sinh học
Natron cũng có một số ứng dụng trong các phản ứng sinh học, đặc biệt là trong các quá trình điều chỉnh độ pH trong các môi trường sinh học như trong cơ thể người. Nhờ tính chất kiềm, Natron giúp duy trì độ pH ổn định trong dạ dày và hỗ trợ quá trình tiêu hóa các thực phẩm có tính axit.

4. Lịch sử phát hiện và nghiên cứu về Natron
Natron là một hợp chất đã được biết đến từ thời cổ đại và có một lịch sử lâu dài trong nhiều nền văn hóa. Nó không chỉ có ứng dụng trong công nghiệp mà còn đóng vai trò quan trọng trong các nghi lễ tôn giáo, y học và đời sống hàng ngày. Dưới đây là một số mốc quan trọng trong lịch sử phát hiện và nghiên cứu về Natron:
4.1. Lịch sử phát hiện Natron và ứng dụng đầu tiên
Natron đã được người Ai Cập cổ đại biết đến và sử dụng từ khoảng 3500 năm trước Công Nguyên. Người Ai Cập không chỉ dùng Natron như một chất tẩy rửa mà còn dùng nó trong các nghi lễ tôn giáo và trong quá trình ướp xác. Họ phát hiện ra rằng Natron có khả năng khử trùng và bảo quản, điều này khiến nó trở thành một phần không thể thiếu trong các quy trình ướp xác mummification.
Trong suốt lịch sử, Natron đã được sử dụng để điều chỉnh độ pH trong các quá trình tẩy rửa, làm sạch và xử lý nước. Ở phương Tây, vào thế kỷ 17 và 18, Natron đã trở thành nguyên liệu phổ biến trong các phòng thí nghiệm hóa học, nơi các nhà khoa học nghiên cứu nó như một chất kiềm mạnh trong các phản ứng hóa học.
4.2. Các nghiên cứu khoa học về Natron qua các thời kỳ
Vào thế kỷ 19, các nhà hóa học bắt đầu nghiên cứu kỹ lưỡng hơn về các tính chất hóa học của Natron, đặc biệt là trong việc tách và sản xuất các muối cacbonat khác từ Natron. Mặc dù Natron đã được sử dụng rộng rãi từ lâu, nhưng chỉ đến khi các phương pháp hóa học hiện đại ra đời, chúng ta mới có thể hiểu rõ về cấu trúc phân tử và các tính chất vật lý của nó.
Trong thế kỷ 20, với sự phát triển của các ngành công nghiệp hóa chất, Natron đã được sử dụng chủ yếu trong sản xuất xà phòng, thủy tinh, chất tẩy rửa và nhiều sản phẩm khác. Các nghiên cứu đã chỉ ra rằng Natron có vai trò quan trọng trong việc giảm nhiệt độ nóng chảy của thủy tinh và là nguyên liệu quan trọng trong sản xuất soda ash (natri cacbonat), một hóa chất công nghiệp thiết yếu.
4.3. Những nghiên cứu gần đây và ứng dụng hiện đại
Ngày nay, Natron tiếp tục là một chủ đề nghiên cứu quan trọng trong các lĩnh vực như hóa học môi trường, công nghệ sinh học và y học. Các nghiên cứu hiện đại đang khám phá khả năng sử dụng Natron trong việc xử lý nước, giảm ô nhiễm môi trường, cũng như trong ngành dược phẩm để điều chỉnh độ pH trong cơ thể người. Ngoài ra, Natron cũng đang được nghiên cứu để phát triển các phương pháp xử lý chất thải công nghiệp và nông nghiệp một cách hiệu quả và bền vững hơn.
5. Natron trong cuộc sống hàng ngày và trong gia đình
Natron không chỉ là một hợp chất quan trọng trong công nghiệp mà còn có rất nhiều ứng dụng hữu ích trong cuộc sống hàng ngày và trong gia đình. Dưới đây là một số cách sử dụng Natron trong việc làm sạch, nấu ăn, chăm sóc sức khỏe và khử mùi trong gia đình:
5.1. Sử dụng Natron trong làm sạch và khử mùi
Natron là một chất tẩy rửa tự nhiên rất hiệu quả, được sử dụng để làm sạch bề mặt trong nhà bếp, nhà vệ sinh và các khu vực khác. Với tính chất kiềm của mình, Natron có khả năng làm mềm nước, giúp loại bỏ các vết bẩn cứng đầu như dầu mỡ, vết ố vàng và các vết bẩn khó tẩy. Bạn có thể sử dụng Natron để:
- Làm sạch bề mặt bếp, đặc biệt là các vết dầu mỡ.
- Tẩy trắng quần áo, đặc biệt là các vết ố vàng trên áo trắng.
- Làm sạch thảm và ghế sofa, khử mùi khó chịu trên thảm.
- Khử mùi tủ lạnh, giúp không khí trong tủ lạnh luôn sạch sẽ và tươi mới.
5.2. Cách sử dụng Natron trong nấu ăn và làm bánh
Natron là một thành phần không thể thiếu trong nhiều công thức nấu ăn và làm bánh, đặc biệt là trong các món nướng. Nhờ vào tính chất kiềm, Natron giúp làm nở bột, tạo ra cấu trúc xốp cho các loại bánh như bánh mì, bánh quy hay bánh ngọt. Dưới đây là một số ứng dụng của Natron trong nấu ăn:
- Thay thế bột nở trong các công thức làm bánh để giúp bánh nở đều và mềm mịn.
- Trung hòa acid trong các món ăn có tính chua, như trong các món cà chua hoặc giấm.
- Sử dụng Natron để làm mềm thịt, giúp thịt trở nên mềm và dễ ăn hơn.
5.3. Natron trong chăm sóc sức khỏe và làm đẹp
Natron cũng có một số ứng dụng trong việc chăm sóc sức khỏe và làm đẹp. Một số công dụng phổ biến của Natron bao gồm:
- Giảm acid dạ dày: Natron có thể giúp trung hòa acid dạ dày, giảm các triệu chứng trào ngược axit hoặc ợ nóng.
- Khử mùi cơ thể: Natron là một chất khử mùi tự nhiên, có thể được sử dụng làm lăn khử mùi cho cơ thể.
- Chăm sóc da: Natron có thể được sử dụng để tẩy tế bào chết cho da, giúp làn da mềm mại và sạch sẽ.
5.4. Sử dụng Natron để làm sạch không khí và khử mùi trong nhà
Natron có khả năng hấp thụ mùi và giúp không gian sống trở nên dễ chịu hơn. Bạn có thể đặt một hộp Natron mở trong phòng để hút ẩm và khử mùi hôi trong nhà, đặc biệt là trong phòng ngủ, nhà bếp hoặc nhà vệ sinh. Ngoài ra, Natron cũng giúp giảm độ ẩm trong các khu vực bị ẩm ướt, ngăn ngừa sự phát triển của nấm mốc và vi khuẩn.
5.5. Natron trong các mẹo vặt gia đình
Ngoài các ứng dụng trên, Natron còn có thể được sử dụng trong nhiều mẹo vặt gia đình khác như:
- Làm sạch đồ dùng bằng bạc: Natron giúp đánh bóng bạc, làm cho đồ trang sức hoặc dụng cụ bằng bạc sáng bóng trở lại.
- Làm sạch bồn tắm và bồn rửa mặt: Natron có thể được sử dụng để làm sạch các vết bẩn trong bồn tắm, giúp các bề mặt sáng bóng và sạch sẽ.
- Giảm mùi hôi giày: Đặt một ít Natron vào giày để khử mùi hôi hiệu quả, đặc biệt là trong những ngày hè nóng bức.
Với các công dụng đa dạng và an toàn, Natron là một sản phẩm vô cùng hữu ích trong mỗi gia đình, giúp tiết kiệm chi phí và bảo vệ sức khỏe cho cả gia đình.

6. Các lưu ý khi sử dụng Natron
Natron là một hợp chất hữu ích với nhiều ứng dụng trong đời sống hàng ngày, công nghiệp và khoa học. Tuy nhiên, khi sử dụng Natron, người dùng cần lưu ý một số điểm quan trọng để đảm bảo an toàn và đạt hiệu quả cao nhất. Dưới đây là một số lưu ý khi sử dụng Natron:
6.1. Lợi ích sức khỏe khi sử dụng Natron đúng cách
- Hỗ trợ tiêu hóa: Natron có thể giúp giảm các triệu chứng ợ nóng, trào ngược axit hoặc khó tiêu. Tuy nhiên, chỉ nên sử dụng một lượng nhỏ và không quá thường xuyên. Việc lạm dụng Natron có thể gây ra vấn đề về cân bằng axit - kiềm trong cơ thể.
- Khử mùi tự nhiên: Natron là một chất khử mùi tự nhiên rất hiệu quả. Bạn có thể sử dụng Natron để khử mùi hôi cơ thể, giày dép hoặc không khí trong phòng. Đặc biệt, Natron rất an toàn khi sử dụng để khử mùi trong tủ lạnh hoặc các vật dụng trong gia đình.
- Chăm sóc da: Natron có thể được dùng để làm sạch da hoặc tẩy tế bào chết. Tuy nhiên, vì tính kiềm của nó, bạn nên thử trước trên một vùng da nhỏ để đảm bảo không gây kích ứng da.
6.2. Những rủi ro và lưu ý khi sử dụng Natron trong công nghiệp
- Chú ý khi tiếp xúc với mắt: Natron có tính kiềm cao và có thể gây kích ứng hoặc tổn thương mắt nếu tiếp xúc trực tiếp. Khi làm việc với Natron trong công nghiệp, luôn sử dụng kính bảo vệ và các thiết bị an toàn khác để tránh tiếp xúc với mắt.
- Tránh hít phải bụi Natron: Bụi Natron có thể gây kích ứng đường hô hấp nếu hít phải. Khi sử dụng Natron trong môi trường công nghiệp, cần có hệ thống thông gió tốt và sử dụng khẩu trang bảo vệ khi cần thiết.
- Giữ Natron xa tầm tay trẻ em: Natron là một chất hóa học có tính kiềm mạnh, nên cần bảo quản nơi khô ráo, thoáng mát và xa tầm tay trẻ em để tránh nguy hiểm khi sử dụng.
6.3. Lưu ý khi sử dụng Natron trong nấu ăn và làm bánh
- Đúng liều lượng: Khi sử dụng Natron trong nấu ăn, đặc biệt là trong các món bánh, hãy chú ý đến liều lượng vì Natron có thể làm thay đổi hương vị nếu sử dụng quá nhiều. Một lượng nhỏ Natron sẽ giúp bột nở đều, nhưng nếu quá nhiều, nó có thể làm món ăn có vị đắng.
- Tránh trộn Natron với các thành phần acid mạnh: Khi trộn Natron với các axit như giấm hoặc chanh trong công thức nấu ăn, cần lưu ý rằng phản ứng giữa Natron và axit sẽ tạo ra khí CO₂, vì vậy phải đảm bảo không sử dụng quá nhiều Natron để tránh tạo ra khí thừa gây khó chịu.
6.4. Bảo quản Natron đúng cách
- Đóng kín bao bì: Natron nên được bảo quản trong bao bì kín để tránh ẩm ướt làm giảm hiệu quả của sản phẩm. Khi Natron tiếp xúc với không khí ẩm, nó có thể bắt đầu phản ứng và mất đi tính hiệu quả.
- Tránh ánh sáng trực tiếp: Để đảm bảo chất lượng, bạn nên bảo quản Natron ở nơi khô ráo, thoáng mát và tránh ánh sáng trực tiếp, vì ánh sáng có thể làm giảm chất lượng của Natron theo thời gian.
Nhìn chung, Natron là một chất an toàn và có nhiều lợi ích, nhưng việc sử dụng đúng cách và tuân thủ các lưu ý trên sẽ giúp tối ưu hóa hiệu quả và đảm bảo an toàn cho người sử dụng.
XEM THÊM:
7. Các bài viết, tài liệu tham khảo và nguồn thông tin thêm
Để tìm hiểu thêm về Natron (Na₂CO₃), công thức hóa học của nó, cũng như các ứng dụng trong đời sống, công nghiệp và nghiên cứu khoa học, bạn có thể tham khảo các tài liệu và nguồn thông tin sau:
7.1. Các nguồn tài liệu nghiên cứu về Natron
- Sách giáo khoa Hóa học: Các sách giáo khoa về Hóa học, đặc biệt là các sách chuyên khảo về hóa học vô cơ, thường cung cấp thông tin chi tiết về các hợp chất hóa học, bao gồm Natron. Những tài liệu này giải thích về tính chất, cấu trúc phân tử và ứng dụng của Natron trong công nghiệp và nghiên cứu.
- Các bài nghiên cứu khoa học: Các bài báo khoa học và nghiên cứu được đăng tải trên các tạp chí chuyên ngành như "Journal of Chemical Engineering", "Industrial & Engineering Chemistry Research" cung cấp thông tin sâu sắc về các nghiên cứu mới nhất liên quan đến Natron và các hợp chất liên quan.
- Thư viện kỹ thuật và sách chuyên ngành: Những tài liệu từ các thư viện kỹ thuật hoặc các sách chuyên ngành về hóa học công nghiệp cũng là nguồn tài liệu quan trọng giúp bạn hiểu rõ hơn về các ứng dụng của Natron trong các quy trình công nghiệp, từ sản xuất xà phòng, thủy tinh cho đến xử lý nước và môi trường.
7.2. Những bài viết, nghiên cứu khoa học liên quan đến Natron
- Bài viết trên các website khoa học: Các website chuyên về hóa học và công nghiệp thường xuyên cập nhật các bài viết về Natron, từ cách sản xuất đến ứng dụng của nó trong các lĩnh vực khác nhau. Ví dụ, các trang như "ScienceDirect", "PubMed" hoặc "Google Scholar" là những nơi lý tưởng để tìm kiếm các bài nghiên cứu khoa học liên quan.
- Bài viết trên các diễn đàn và blog chuyên ngành: Ngoài các tài liệu nghiên cứu chính thức, bạn cũng có thể tìm thấy những bài viết chia sẻ kinh nghiệm về việc sử dụng Natron trong công nghiệp và đời sống trên các diễn đàn hoặc blog chuyên ngành. Đây là những tài liệu tham khảo bổ sung, giúp bạn hiểu rõ hơn về thực tế sử dụng Natron trong các tình huống cụ thể.
- Báo cáo và tài liệu từ các tổ chức nghiên cứu: Các tổ chức nghiên cứu khoa học quốc tế như Viện Hóa học Hoa Kỳ (American Chemical Society) hoặc Viện Khoa học và Công nghệ Việt Nam (VAST) thường xuyên phát hành báo cáo về các nghiên cứu về Natron và các hợp chất hóa học liên quan. Những báo cáo này có thể cung cấp thông tin giá trị về các nghiên cứu ứng dụng mới nhất.
7.3. Các nguồn thông tin bổ sung khác
- Khoá học trực tuyến: Các khóa học trực tuyến về hóa học và khoa học vật liệu trên các nền tảng như Coursera, edX hoặc Udemy cung cấp các bài học chuyên sâu về Natron và các hợp chất hóa học khác. Đây là những nguồn học tập tuyệt vời cho những ai muốn tìm hiểu thêm về ứng dụng của Natron trong nhiều lĩnh vực.
- Các bài giảng từ các trường đại học: Các bài giảng và tài liệu tham khảo từ các trường đại học nổi tiếng như Đại học Harvard, Đại học Stanford hoặc các trường đại học lớn tại Việt Nam có thể cung cấp những kiến thức sâu rộng về Natron, từ lịch sử phát hiện đến ứng dụng trong công nghiệp và môi trường.
Với những tài liệu và nguồn thông tin trên, bạn sẽ có thể mở rộng kiến thức về Natron, hiểu rõ hơn về tầm quan trọng của nó trong các lĩnh vực nghiên cứu và ứng dụng, đồng thời áp dụng các kiến thức này vào thực tế một cách hiệu quả.























 Blender Room - Cách Tạo Không Gian 3D Tuyệt Đẹp Bằng Blender
Blender Room - Cách Tạo Không Gian 3D Tuyệt Đẹp Bằng Blender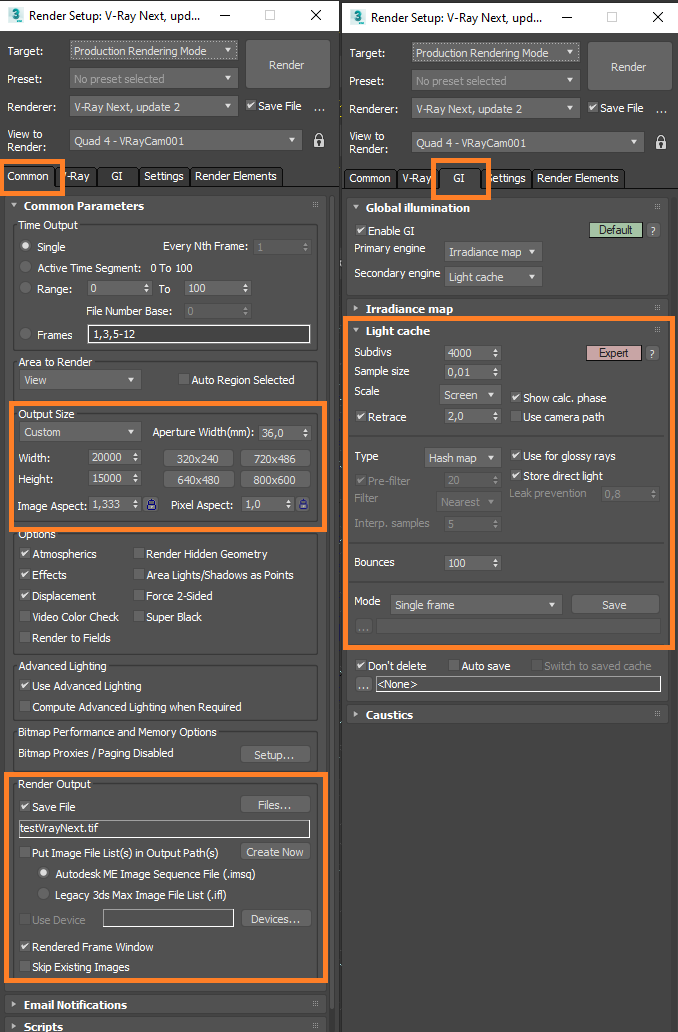 Setting V-Ray 5 Cho 3ds Max: Hướng Dẫn Tối Ưu Hiệu Quả Render
Setting V-Ray 5 Cho 3ds Max: Hướng Dẫn Tối Ưu Hiệu Quả Render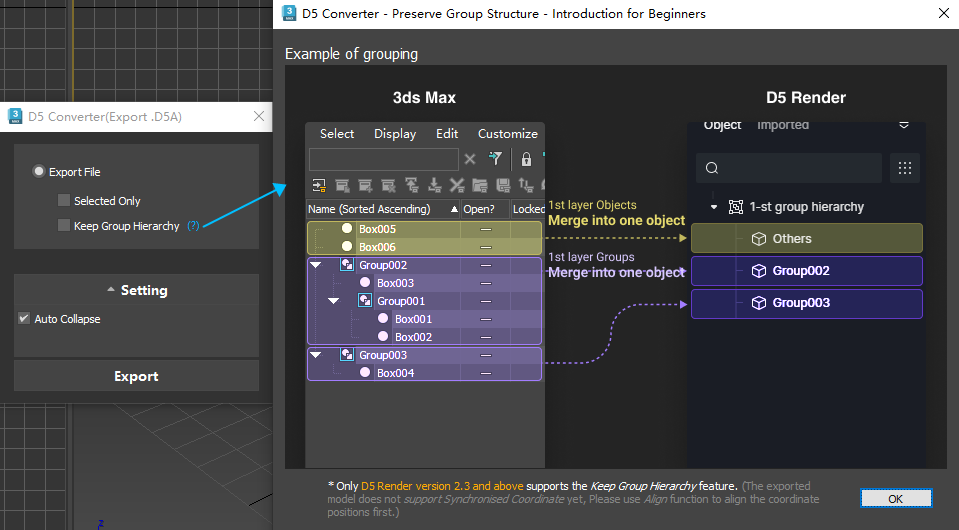 D5 Converter 3ds Max: Hướng Dẫn Chi Tiết Và Các Tính Năng Nổi Bật
D5 Converter 3ds Max: Hướng Dẫn Chi Tiết Và Các Tính Năng Nổi Bật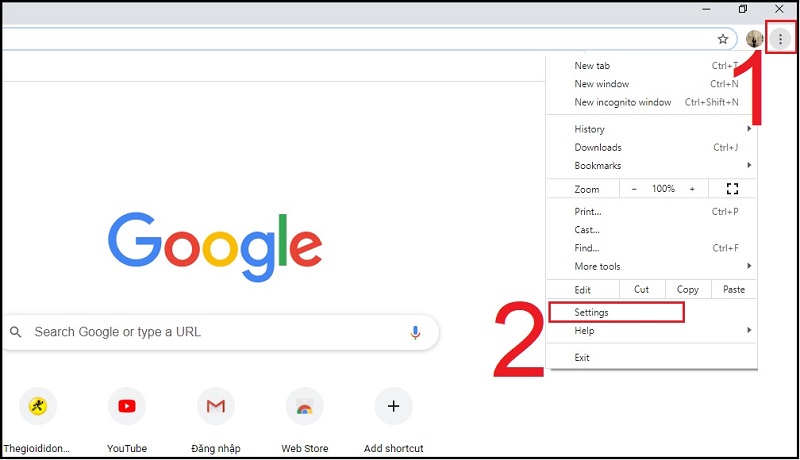 Xóa Lịch Sử Chrome Trên Máy Tính: Hướng Dẫn Chi Tiết Và Hiệu Quả
Xóa Lịch Sử Chrome Trên Máy Tính: Hướng Dẫn Chi Tiết Và Hiệu Quả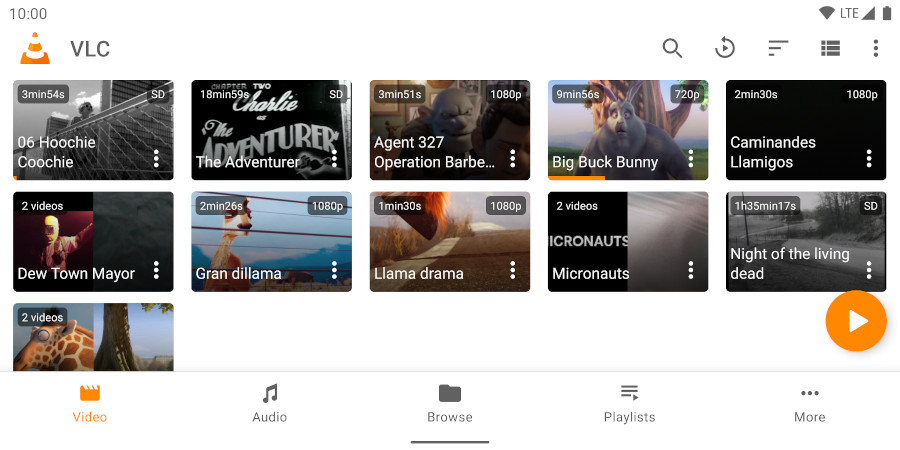 VLC Media Player Android: Hướng Dẫn Chi Tiết và Tính Năng Nổi Bật
VLC Media Player Android: Hướng Dẫn Chi Tiết và Tính Năng Nổi Bật Chuyển File Canva Sang AI: Hướng Dẫn Nhanh Chóng và Đơn Giản Cho Người Mới Bắt Đầu
Chuyển File Canva Sang AI: Hướng Dẫn Nhanh Chóng và Đơn Giản Cho Người Mới Bắt Đầu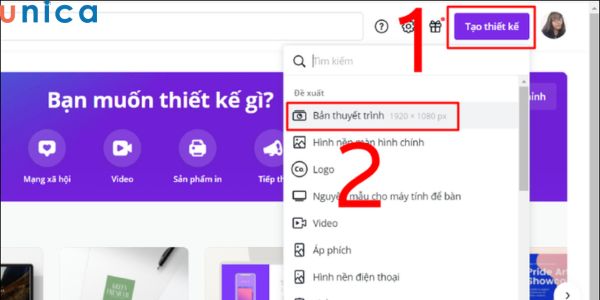 Chuyển từ Canva sang PowerPoint - Hướng dẫn chi tiết và hiệu quả
Chuyển từ Canva sang PowerPoint - Hướng dẫn chi tiết và hiệu quả Ghi Âm Zoom Trên Máy Tính: Hướng Dẫn Chi Tiết và Mẹo Hữu Ích
Ghi Âm Zoom Trên Máy Tính: Hướng Dẫn Chi Tiết và Mẹo Hữu Ích "Notion có tiếng Việt không?" - Hướng dẫn thiết lập và lợi ích khi sử dụng
"Notion có tiếng Việt không?" - Hướng dẫn thiết lập và lợi ích khi sử dụng Facebook No Ads XDA - Trải Nghiệm Không Quảng Cáo Đáng Thử
Facebook No Ads XDA - Trải Nghiệm Không Quảng Cáo Đáng Thử Autocad Alert: Giải Pháp Toàn Diện cho Mọi Thông Báo và Lỗi Thường Gặp
Autocad Alert: Giải Pháp Toàn Diện cho Mọi Thông Báo và Lỗi Thường Gặp Ký Hiệu Trên Bản Vẽ AutoCAD: Hướng Dẫn Toàn Diện và Thực Hành
Ký Hiệu Trên Bản Vẽ AutoCAD: Hướng Dẫn Toàn Diện và Thực Hành Tổng hợp lisp phục vụ bóc tách khối lượng xây dựng
Tổng hợp lisp phục vụ bóc tách khối lượng xây dựng Chỉnh kích thước số dim trong cad – cách đơn giản nhất 2024
Chỉnh kích thước số dim trong cad – cách đơn giản nhất 2024